Recomendado para usted
Desafío
- La contaminación durante el envasado de inyectables estériles estaba provocando pérdidas de dos dígitos de los lotes por año.
Soluciones
- Inteligencia de fabricación: - las aplicaciones de software FactoryTalk almacenan, organizan y muestran los datos del sistema de control para automatizar la generación informes para la FDA, presentar informes personalizados y asegurar el control de calidad.
- Inteligencia de fabricación: - Automated Systems Inc. combina conocimientos profundos de la industria con gestión de proyectos y diseño, configuración, implementación y validación del sistema.
Resultados
- Ahorró por lo menos USD 250,000 por año al reducir las pérdidas en los lotes a cero.
- El monitoreo remoto de supervisión de estado del lote permite que un solo operador asista muchos procesos.
- Los informes almacenados en formato PDF permiten la localización del lote.
- Los datos históricos están disponibles para el análisis de tendencias y procesos.
- Los informes de tablero configurados con indicadores clave de rendimiento basados en roles brindan a los operadores y los gerentes información en tiempo real, factible y clara.
Antecedentes
Muchos medicamentos vitales son escasos en los Estados Unidos, una situación que desató la queja de los pacientes e incluso audiencias ante el congreso. Los líquidos que reciben los pacientes, ya sea por inyección o de manera intravenosa, encabezan la lista de medicamentos de necesidad crítica. De hecho, cerca del 75 por ciento de los medicamentos en la lista federal de faltantes de la Dirección de Alimentos y Medicamentos de los Estados Unidos son líquidos, como aquellos para quimioterapia, anestesias y soluciones nutricionales.
Los expertos de la industria y de la FDA están de acuerdo con que una gran parte del problema es el proceso exigente y a menudo complejo que se necesita para proteger la pureza del medicamento durante la producción. Solo en 2010, más de la mitad de los lotes de medicamentos inyectables producidos por fabricantes farmacéuticos se descartaban por problemas de calidad, como contaminación bacteriana e impurezas de partículas industriales.
La historia de un fabricante muestra la gravedad de la situación y cómo las empresas pueden utilizar la tecnología automatizada para ayudar a superarla.
Desafío
En un año, la contaminación en una línea de envasado generó pérdidas de lotes de dos dígitos para este productor de inyectables estériles radicado en Estados Unidos. El problema en el proceso ocurrió durante la transferencia de medicamentos desde el buque a granel a los viales plásticos mediante una máquina de soplado, llenado y sellado.
Para asegurar que todo el equipo estuviera esterilizado antes de introducir el medicamento, el operador aplicó presión a la línea al abrir y cerrar manualmente una serie de 20 a 30 válvulas durante el proceso. Esto eliminó el aire exterior y los contaminantes. Pero abrir una válvula fuera de la secuencia o en el momento incorrecto puede comprometer el lote.
El error humano no fue el único problema. Los defectos en el sellado de una válvula o en el acoplamiento de instrumentos también podrían ocasionar un pérdida de presión y afectar la pureza del producto. A la línea también le faltaba un sistema de alarmas que señalara fallos potenciales, por lo que los operadores de la planta no sabían si tenían un lote malo hasta que se probara el producto final.
Solución
En la búsqueda de una solución integral, el fabricante de medicamentos aprovechó Automated Systems Inc. (ASI) para actualizar su sistema de control y visualización. ASI creó un sistema para contener de manera automática la contaminación en la línea, el cual emite alarmas cuando cualquier parámetro del proceso varía fuera del rango preseleccionado, y rastrea y registra los datos claves del proceso para verificar la esterilidad de cada lote terminado.
La solución dependía de una estrategia de inteligencia de fabricación basada en hardware y software de Rockwell Automation. Gracias al nuevo controlador de automatización programable ControlLogix® de Allen-Bradley®, los ingenieros de ASI diseñaron un sistema que predetermina todos los pasos de secuenciación y procesamiento, incluido el procedimiento crucial de presurización.
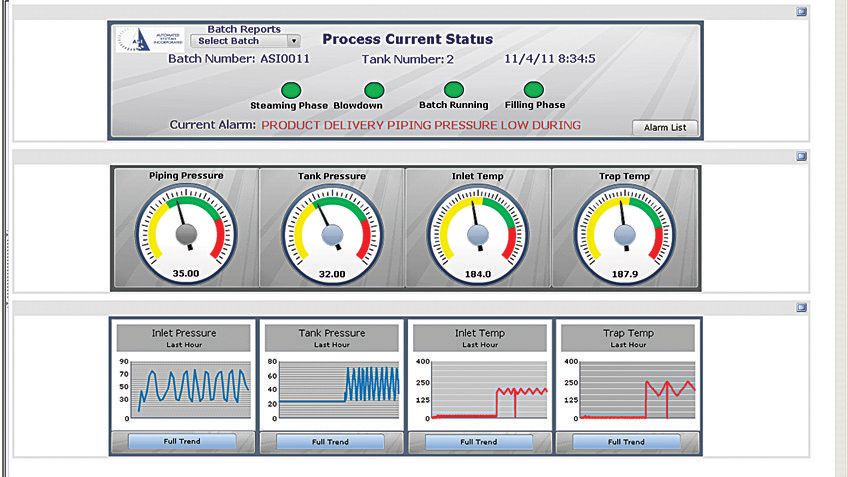
El sistema incorporó el software FactoryTalk de Rockwell Automation, incluida una interface operador-máquina (HMI) que ejecuta el software FactoryTalk® View Site Edition (SE). La HMI muestra el estado en tiempo real del sistema en una sofisticada pantalla de simulación. Esta pantalla (a la que también se puede acceder a través de un explorador web seguro para monitoreo remoto) brinda al operador una descripción detallada del estado de cada válvula del sistema, junto con las lecturas de presión y temperatura.
Esto permite al operador realizar la operación indicada de manera rápida y correcta con conocimiento profundo del sistema entero. El software FactoryTalk View SE hace que el operador realice algunas acciones y verifique las variables en cada paso del proceso. Si se presenta una advertencia o alarma, el sistema identifica automáticamente la ubicación potencial del fallo, aísla el producto allí y vuelve a esterilizar la línea.
Para mejorar el registro y simplificar la generación de informes, ASI incorporó FactoryTalk Historian y el software VantagePoint EMI en el nuevo sistema. Juntas, las aplicaciones rastrean y generan informes sobre los parámetros y las alarmas en todos los procesos críticos. Ahora, los operadores tienen acceso en tiempo real a los datos de producción críticos desde interfaces, tableros e informes generados de manera automática, para que puedan desactivar cualquier problema potencial de producción antes de que ocurra. Los gerentes comerciales, por su parte, pueden evaluar los datos históricos para tomar decisiones mejor informadas.
Al final de cada ciclo de operación, el nuevo sistema genera de manera automática un informe con una lista de cualquier alarma o condición que afecte la esterilidad. Si los operadores detectan una anomalía, pueden consultar los datos históricos para reconocer exactamente dónde ocurrió el error y trabajar rápidamente para resolver la situación. Los datos de producción de rastreo automático también eliminan la necesidad de probar cada lote al final el proceso.
Los informes se almacenan en formato PDF para proporcionar la localización del lote. Los operadores y los gerentes de la planta utilizan los datos históricos para realizar análisis de procesos y tendencias.
FactoryTalk Historian y el software VantagePoint EMI también satisfacen los requisitos normativos de generación de informes. FactoryTalk Historian actúa como repositorio de registros seguro que permite al fabricante cumplir las reglas de registros electrónicos de la FDA. FactoryTalk VantagePoint EMI permite al sistema correlacionar datos de respaldo del registro del lote, lo cual mejora el cumplimiento con los reglamentos de buenas prácticas de fabricación actuales de la entidad.
Resultado
Desde que se implementó el nuevo sistema, el fabricante no ha perdido un solo lote por contaminación. Cada lote terminado vale más de USD 250,000, por lo que la inversión en el nuevo sistema se paga por sí sola rápidamente.
La empresa también gastó menos tiempo y dinero para cumplir con los reglamentos de generación de informes de la FDA porque el sistema realiza un seguimiento de la seguridad del lote automáticamente.
Los pacientes también se beneficiaron, al recibir más cantidad del medicamento que necesitan.
Publicado 28 de mayo de 2015