Recommandé pour vous
Les histoires d’accident - et pire – de patients victimes de médicaments falsifiés ou d'instruments médicaux issus de la contrefaçons, continuent de faire la une des journaux.
Des experts de l'Agence Nationale pour la Sécurité du Médicament et des produits de santé (ANSM) estiment que les deux tiers des produits pharmaceutiques vendus sur des sites Web non réglementés ne sont pas conformes aux exigences de qualité. Cela suscite clairement des craintes quant au danger potentiel pour les consommateurs. Et les entreprises pharmaceutiques sont à juste titre inquiètes de l'effet que ces sites ont, ou auront bientôt, sur leurs propres revenus et profits. Pas étonnant que tout le monde s’accorde sur la nécessité de minimiser les risques en mettant en œuvre les bonnes pratiques et solutions.
La nouvelle directive de l'Union Européenne visant à réduire le risque de falsification des produits dans la chaîne d'approvisionnement entrera en vigueur d'ici deux ans. Mais comme la réglementation de l'UE donne peu d'indications sur ce qu'elle considère comme une solution appropriée, les entreprises pharmaceutiques se demandent encore comment aborder ce défi majeur.
Dans ce contexte, nous travaillons actuellement en France pour conseiller et accompagner les laboratoires pharmaceutiques et d'autres sociétés spécialisées dans les sciences de la vie afin de faire la transition vers le suivi et la traçabilité automatisés de leurs produits.
Ils réalisent qu'ils doivent commencer à planifier leurs opérations pour assurer la conformité - et pour protéger leur marque.
Au cours des derniers mois, il est intéressant de noter que la modernisation de notre industrie, à travers l'initiative Industrie Du Futur, devient progressivement plus importante aux yeux de notre gouvernement et dans les programmes (des candidats à la prochaine élection présidentielle en France).
L’objectif est de relancer l’économie française et de rendre le pays plus compétitif.
Nous remarquons que les clients sont très intéressés par notre nouvelle solution de sérialisation. C'est parce que nous n’aidons pas uniquement les entreprises à mettre en œuvre la traçabilité de bout en bout de la chaine logistique pour se conformer à la directive à venir. Nous leur donnons également, et surtout, les moyens de rationaliser et d'optimiser chaque phase de leur chaîne de production, de l'usine jusqu’au Cloud. Notre solution de sérialisation fait partie d'une approche holistique, la solution Connected Enterprise, qui aide les entreprises dans leur transition vers l'Industrie du Futur. Au niveau le plus élémentaire, la valeur de la solution Connected Enterprise consiste à interconnecter les capteurs, les machines, les équipements d'une usine de fabrication, à les contrôler à l'aide de logiciels intelligents et à transformer les données de production en informations intelligentes permettant aux utilisateurs de prendre des décisions rapides et efficaces.
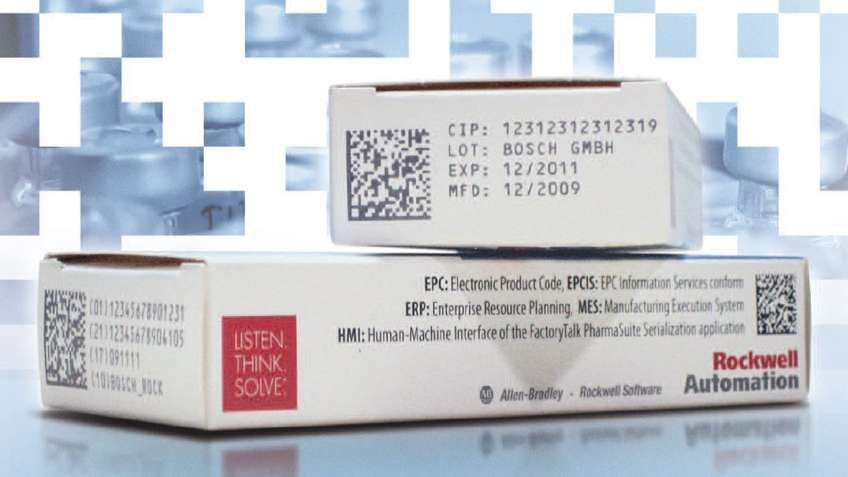
La solution de sérialisation de Rockwell Automation est basée sur une plate-forme industrielle modulaire et évolutive de contrôle et d'information qui peut être facilement intégrée aux lignes de production existantes des fabricants de produits pharmaceutiques et médicaux. Bien que notre solution de sérialisation sépare complètement le contrôle de la machine et les fonctionnalités de gestion de données, elle peut également étendre l'intégration au-delà de l'usine pour englober aussi le niveau de l'entreprise (du niveau 0 au niveau 5). Cela donne aux clients une solution centralisée pour la gestion des données de sérialisation dans l'ensemble de l’entreprise et facilite la traçabilité des produits tout au long de la chaîne d'approvisionnement. Une des raisons pour lesquelles nous voyons un tel intérêt pour cette solution en France, c'est qu'elle offre une gamme d'avantages commerciaux qui vont au-delà de la lutte contre la contrefaçon. Et notre approche holistique avec la solution Connected Enterprise signifie que notre solution de sérialisation dépasse le simple niveau de l’usine - elle couvre bien plus que les imprimantes d'étiquettes tamper evident et de codes-barres CIP 13.
Les avantages comprennent une visibilité accrue tout au long de la chaîne d'approvisionnement, permettant aux fabricants d'ajuster leur production et leurs stocks en fonction de la demande des marchés. Grâce à cette souplesse et à cette agilité accrues, ils peuvent plus facilement répondre aux changements de consommation en temps réel.
Une plus grande visibilité signifie également qu'il est plus facile pour les fabricants de produits et d’équipements pharmaceutiques de gérer et de contenir les rappels de produits.
Comme les plateformes de contrôle et d'information sont intégrées, l'information peut être partagée entre les systèmes de contrôle, les systèmes de gestion de la production (MES), les systèmes informatiques d'entreprise (ERP), la gestion des stocks et les systèmes de la supply chain. Cette ouverture assure également que les données de sérialisation peuvent être utilisées pour étayer les activités commerciales stratégiques, telles que la planification financière et commerciale ou la mise sur le marché.
La solution est conçue et construite autour de standards ouverts et communs, y compris les normes IEC 61131, ANSI / ISA-88 et ANSI / ISA-95, ainsi que les protocoles de réseau ouvert et sécurisé tels que Ethernet IP. Cela facilite l'intégration dans la plupart des environnements d'usines, élimine les solutions de contrôle propriétaires exclusives et les interfaces personnalisées associées, et fournit un rapport temps-valeur et retour sur investissement rapide.
Compte tenu du statut de la France sur le marché médical mondial - en tant que l'un des plus grands producteurs, ainsi que d'une importante consommation par habitant en termes financiers - les enjeux sont particulièrement élevés dans notre pays.
Le marché pharmaceutique et médical est également un facteur majeur de la croissance économique de la France. Dans cette perspective, la mise en œuvre de technologies de sérialisation efficaces ne peut pas attendre, car elle affecte directement des millions de patients et des centaines d'entreprises.
Publié 27 février 2017