Consigliato
Sfida
- Problemi di contaminazione durante la fase di confezionamento di farmaci iniettabili hanno causato ogni anno perdite di lotti ingenti.
Soluzioni
- Informazioni di produzione - Le applicazioni software FactoryTalk consentono di archiviare, organizzare e visualizzare dati dal sistema di controllo per automatizzare la reportistica FDA, generare report personalizzati e garantire il controllo della qualità.
- Informazioni di produzione - Automated Systems Inc. ha una vasta competenza nel settore e offre servizi di progettazione, configurazione, implementazione e convalida di sistemi e di gestione dei progetti.
Risultati
- Risparmio di almeno 250.000 $ all'anno grazie all'azzeramento delle perdite di lotti
- Monitoraggio remoto dello stato dei lotti che consente la gestione di diversi processi da parte di un solo operatore.
- Report in formato PDF per la tracciabilità dei lotti
- Dati storici disponibili per l'analisi di andamenti e processi
- Report configurati con KPI basati sul ruolo forniscono informazioni chiare, utili e in tempo reale a operatori e dirigenti.
Contesto
Negli Stati Uniti, le scorte di molti medicinali salvavita sono insufficienti e questa situazione ha provocato le proteste dei pazienti e persino dibattiti al Congresso. I farmaci di cui si ha maggiore necessità sono i medicinali liquidi che i pazienti ricevono tramite iniezione o per via endovenosa. In effetti, quasi il 75% dei farmaci inclusi nella lista dei medicinali scarseggianti stilata dalla Food and Drug Administration sono liquidi, ovvero chemioterapici, anestetici e soluzioni nutrizionali.
La FDA e gli esperti del settore sono concordi nel ritenere che il problema è dovuto anche alla rigorosa e spesso complessa procedura necessaria per proteggere la purezza del farmaco durante la fase di produzione. Nel 2010, più della metà dei lotti di farmaci iniettabili prodotti da aziende farmaceutiche è stata scartata a causa di problemi di qualità come contaminazione batterica e impurità particellari.
Quanto descritto nel presente documento illustra la gravità della situazione e il modo in cui le aziende possono risolvere il problema avvalendosi di tecnologie automatizzate.
Sfida
La contaminazione sulla linea di confezionamento ha provocato ogni anno perdite di lotti a doppia cifra per questo produttore di farmaci iniettabili sterili basato negli Stati Uniti. Il problema si verificava durante il trasferimento del medicinale da contenitori di grandi dimensioni in fiale di plastica mediante una macchina BFS.
Per garantire la sterilità di tutte le macchine prima dell'introduzione del farmaco, l'operatore pressurizzava manualmente la linea aprendo e chiudendo una serie di 20-30 valvole durante il processo. In questo modo, si eliminavano l'aria esterna e i contaminanti. Tuttavia, l'apertura fuori sequenza o al momento sbagliato di una valvola poteva compromettere la purezza del lotto.
L'errore umano non era comunque il solo problema, in quanto anche una guarnizione o un giunto difettoso poteva comportare una perdita di pressione e la contaminazione del prodotto. Inoltre, la linea non includeva un sistema di allarme per segnalare potenziali guasti, di conseguenza gli operatori non sapevano se il lotto era inutilizzabile fino a che non veniva verificato.
Soluzione
L'azienda aveva bisogno di una soluzione completa e si è rivolta a Automated Systems Inc. (ASI) per aggiornare il sistema di controllo e visualizzazione. ASI ha quindi creato un sistema per limitare automaticamente la contaminazione sulla linea, generare allarmi ogni volta che un parametro non rientra nei range predefiniti nonché monitorare e registrare i dati di processo essenziali per verificare la sterilità di ogni lotto completato.
La soluzione utilizza una strategia di informazioni di produzione basata su hardware e software di Rockwell Automation. Avvalendosi di un nuovo controllore di automazione programmabile Allen-Bradley® ControlLogix®, i tecnici ASI hanno progettato un sistema che predetermina tutte le fasi di elaborazione e sequenziamento, inclusa quella più cruciale, vale a dire la fase di pressurizzazione.
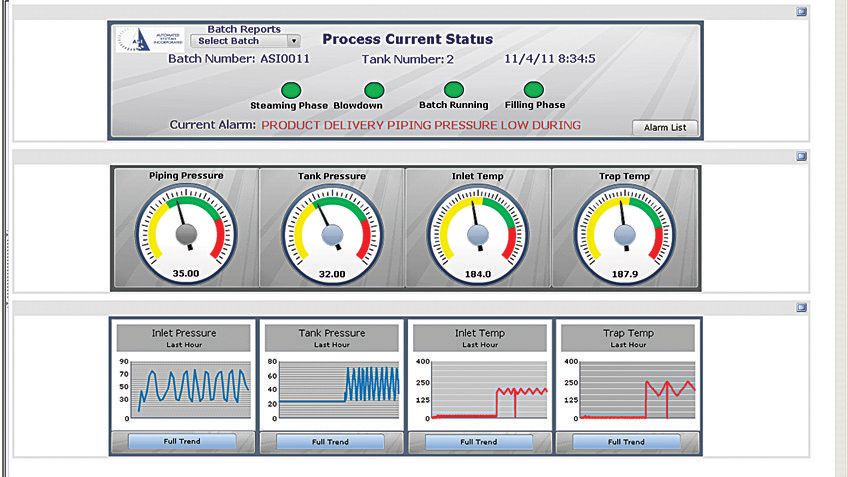
Il sistema include il software FactoryTalk di Rockwell Automation, tra cui un'interfaccia operatore (HMI) in cui è in esecuzione il software FactoryTalk® View Site Edition (SE). L'interfaccia mostra lo stato in tempo reale del sistema in una schermata avanzata, accessibile anche da un browser Web protetto per il monitoraggio remoto, che fornisce agli operatori una panoramica dettagliata dello stato di ogni valvola nel sistema nonché i valori di pressione e temperatura.
Disponendo di informazioni chiare e precise sull'intero sistema, l'operatore può eseguire rapidamente e correttamente l'operazione appropriata. Il software FactoryTalk View SE richiede all'operatore di eseguire determinate azioni e di verificare le variabili in ogni fase del processo. In caso di avviso o allarme, il sistema identifica automaticamente il punto in cui è avvenuto il problema, isola il prodotto in quell'area e sterilizza di nuovo la linea.
Per migliorare la gestione dei record e semplificare la reportistica, ASI ha incorporato nel nuovo sistema i software FactoryTalk Historian e VantagePoint EMI, che consentono di monitorare e documentare tutti i parametri e gli allarmi di processo critici. Ora gli operatori hanno accesso in tempo reale ai dati di produzione essenziali tramite interfacce, dashboard e report generati automaticamente, e sono quindi in grado di prevenire qualsiasi potenziale problema di produzione. I business manager possono inoltre analizzare i dati storici per prendere decisioni più informate.
Alla fine di ogni ciclo operativo, il nuovo sistema genera automaticamente un report che elenca tutti gli allarmi o le condizioni relativi alla sterilità. Se gli operatori notano un'anomalia, sono in grado di determinare in modo esatto, grazie ai dati storici, dove si è verificato l'errore e agire prontamente per correggere la situazione. Il monitoraggio automatico dei dati di produzione elimina inoltre la necessità di verificare ogni lotto alla fine del processo.
I report sono archiviati in formato PDF per consentire la tracciabilità dei lotti. I manager e gli operatori dell'impianto utilizzano i dati storici per analizzare andamenti e processi.
I software FactoryTalk Historian e VantagePoint EMI soddisfano inoltre i requisiti di reportistica normativa. FactoryTalk Historian è un repository di record sicuro che consente all'azienda di ottemperare alle normative sui record elettronici della FDA. FactoryTalk VantagePoint EMI consente al sistema di correlare dati di supporto attendibili per il record di lotto, migliorando la conformità alle norme di buona fabbricazione correnti della FDA.
Risultato
Dalla data di implementazione del nuovo sistema, l'azienda non ha perso un solo lotto a causa di problemi di contaminazione. Il valore di ogni lotto finito è superiore a 250.000 $, di conseguenza il costo del nuovo sistema è stato ammortizzato in breve tempo.
L'azienda spende inoltre meno tempo e denaro per conformarsi alle normative di reportistica della FDA, in quanto il sistema monitora automaticamente la purezza dei lotti.
Anche i pazienti beneficiano della soluzione adottata poiché la quantità di farmaci disponibile è maggiore di quella richiesta.
Pubblicato 28 maggio 2015